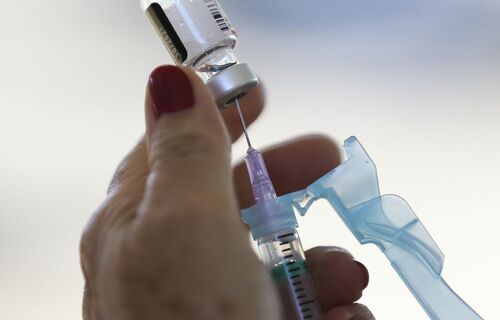
A decisão temporária visa acelerar o acesso à vacinação no Brasil, mantendo a proteção enquanto o registro definitivo é analisado.
A Anvisa renovou a dispensa de registro em caráter excepcional e temporário para duas vacinas contra a monkeypox, em decisão assinada pelo presidente Antônio Barra. A medida, válida por 180 dias a partir de 23 de agosto de 2024, visa agilizar o acesso à vacinação no Brasil. A autorização temporária mantém as vacinas disponíveis enquanto seu registro definitivo não é concedido, garantindo que a imunização prossiga em ritmo acelerado.
O médico infectologista do Centro de Segurança Assistencial (CSA) do Hospital Anchieta Dr. Manuel Palacios explica que, apesar da dispensa de registro, as vacinas passaram por rigorosos testes de segurança antes de serem aplicadas em caráter emergencial.
“A dispensa do registro concedida pela Anvisa é uma medida excepcional que permite o uso de vacinas que já passaram por etapas rigorosas de avaliação de segurança e eficácia em outros países. Essas vacinas já foram aprovadas por agências reguladoras internacionais de alta credibilidade, como é o caso do FDA nos Estados Unidos e a EMA na Europa. Portanto, apesar de não ter o registro completo no Brasil, essas vacinas possuem um perfil de segurança bem estabelecido e são usadas globalmente para combater surtos de Mpox.” Explica.
A renovação se aplica à vacina Jynneos (EUA) ou Imvanex (EMA) – vacina contra varíola e monkeypox, vírus vaccínia modificado, cepa Ankara –, que, apesar de ser o mesmo produto, possui nomes diferentes nos EUA e na Europa. A vacina da empresa Bavarian Nordic A/S é fabricada na Dinamarca e na Alemanha. O imunizante é destinado a adultos com idade igual ou superior a 18 anos e possui prazo de até 60 meses de validade, quando conservado entre -60°C a -40°C.
O que é Mpox?
A monkeypox, também conhecida como Mpox, é uma doença zoonótica viral que pode ser transmitida para humanos através do contato com animais infectados, pessoas contaminadas ou materiais infectados. Os sintomas incluem erupções cutâneas, linfonodos inchados, febre e dores no corpo. Desde o surgimento da doença no Brasil, a vacinação tem sido essencial para conter a disseminação do vírus, que pode causar sérias complicações de saúde. O infectologista Manuel Palacios fala sobre a importância da vacinação.
“A vacinação desempenha um papel crucial na contenção da Mpox no Brasil, especialmente no cenário onde o número de casos está aumentando. A vacina é uma ferramenta fundamental para interromper a transmissão do vírus, protegendo os grupos de risco, como é o caso dos profissionais de saúde, pessoas que tiveram contato próximo com infectados e populações vulneráveis. Com base nos números atuais de casos, a vacina ajuda a prevenir o surgimento de novos focos de transmissão e reduzir a gravidade da doença nos indivíduos vacinados, o que por sua vez diminui a carga sobre o sistema de saúde.”
Atualização dos Casos de Monkeypox no Brasil
Em 2024, foram registrados 709 casos confirmados ou prováveis de monkeypox no Brasil, com 85% dos casos envolvendo homens e 42,2% sendo pessoas que vivem com HIV/Aids. O número representa uma queda significativa em comparação com os mais de 10 mil casos notificados em 2022, no auge do surto. Desde o início da pandemia, 16 óbitos foram confirmados, com o mais recente ocorrido em abril de 2023. As regiões mais afetadas incluem grandes centros urbanos do Sudeste e Nordeste.
Manuel Palacios destaca que a renovação da dispensa de registro é crucial para garantir a continuidade do combate à monkeypox.
“Se a dispensa de registro não fosse renovada, a vacinação contra Mpox no Brasil poderia ser severamente impactada. Sem essa dispensa, as vacinas atualmente utilizadas perderiam a autorização temporária de uso, o que resultaria na interrupção das campanhas de imunização. Isso poderia levar a um aumento na transmissão do vírus, especialmente em áreas com maior incidência de casos. Além disso, a falta de vacinação poderia sobrecarregar o sistema de saúde com mais casos graves e complicações, afetando negativamente a capacidade do país de controlar o surto.”
Em casos de dispensa de registro temporária, a agência reguladora avalia a necessidade de renovação ou aprovação definitiva com base na eficácia e segurança comprovadas das vacinas durante o período de dispensa.
Fonte: Brasil 61